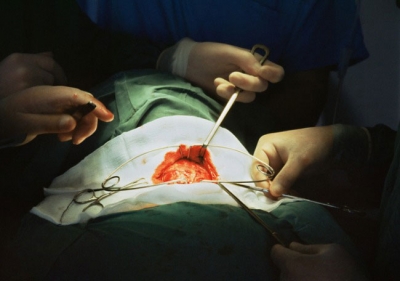
El objetivo primario de este estudio fue evaluar prospectivamente la prevalencia de la paresia incidental preoperatoria de la cuerda vocal y la tasa de incidencia de la lesión perioperatoria del nervio laríngeo recurrente, utilizando una detección laringoscópica rutinaria, antes y después de la cirugía tiroidea
La paresia de la cuerda vocal (PCV) causada por la lesión del nervio laríngeo recurrente (NLR) es una complicación bien conocida de la cirugía tiroidea y ha sido ampliamente documentada en la bibliografía. No obstante, una revisión sistemática de Jeannon y col., demostró una amplia variación en los métodos de detección y en las tasas de PCV entre los estudios previamente publicados.
Las tasas de PCV temporaria van desde el 1,4% al 38,4% (media 9,8%), y desde 0% a 18,6% (media 2,3%) para la PCV permanente [1]. La incidencia de PCV puede ser subestimada a menos que se realice una evaluación rutinaria de la cuerda vocal.
En un estudio involucrando a 26 hospitales escandinavos con 3660 operaciones tiroideas registradas, las instituciones que practicaron una laringoscopía postoperatoria de rutina, reportaron tasas casi dos veces mayores de PCV que aquellas que no lo hicieron [2].
La lesión postoperatoria del NLR es considerada permanente si la inmovilidad o disfunción completa de la cuerda vocal dura más de 1 año [3].
Las lesiones permanentes han sido documentadas en hasta el 1,4%, y las lesiones transitorias en el 5,2–12,6% de los pacientes, de acuerdo con los estudios que utilizaron el examen postoperatorio rutinario de la cuerda vocal [4,5].
Los factores de riesgo reportados para la lesión intraoperatoria del NLR incluyen la edad avanzada, bocio intratorácico, tirotoxicosis, enfermedad maligna tiroidea, tiroidectomía previa, reoperación por sangrado, cirugía extensa, volumen hospitalario de casos bajo o medio, y volumen bajo de casos del cirujano [2,5-8].
El objetivo primario de este estudio fue evaluar prospectivamente la prevalencia de la paresia incidental preoperatoria de la cuerda vocal y la tasa de incidencia de la lesión perioperatoria del NLR, utilizando una detección laringoscópica rutinaria, antes y después de la cirugía tiroidea.
Los objetivos secundarios fueron identificar los factores de riesgo para la lesión del NLR y analizar el resultado de la PCV postoperatoria durante un seguimiento de 12 meses.
| Material y métodos |
> Pacientes del estudio
Se trató de un estudio observacional de una única institución basado en datos recolectados prospectivamente. El comité local de ética aprobó este estudio y no se requirió consentimiento informado de los pacientes.
Todos los pacientes consecutivos que fueron sometidos a una cirugía tiroidea nueva o repetida, entre enero de 2011 y diciembre de 2016, fueron registrados prospectivamente en una base de datos electrónica, como parte de una iniciativa de calidad quirúrgica, en un esfuerzo por mejorar la atención del paciente.
Los datos del seguimiento alejado para el análisis final fueron recolectados retrospectivamente hasta los 12 meses del postoperatorio.
Todos los pacientes remitidos para evaluación quirúrgica electiva fueron sometidos a examen clínico, ecografía tiroidea y biopsia por aspiración con aguja fina (BAAF), cuando fue apropiado. Las indicaciones para la cirugía fueron registradas como; bocio primario, bocio recidivado (cirugía tiroidea previa), nódulo tiroideo sospechoso, nódulo tiroideo maligno, completar la tiroidectomía, hipertiroidismo, u otra indicación.
“Nódulo tiroideo sospechoso” fue definido como neoplasia folicular, o sospecha clínica de malignidad (basada en el tamaño, apariencia, o tasa de crecimiento en la imagen ecográfica), cuando una BAAF no fue concluyente [9].
Los pacientes con nódulo tiroideo sospechoso fueron sometidos a hemitiroidectomía. Se completó la tiroidectomía en un segundo tiempo si se comprobaba que el nódulo removido era maligno.
La indicación para la cirugía fue definida como “nódulo tiroideo maligno” cuando la BAAF preoperatoria fue claramente maligna, de acuerdo con el sistema Bethesda [10].
La hipocalcemia postoperatoria fue definida como calcio sérico ionizado por debajo de 1,16 mmol/L por más de 2 días postoperatorios, requiriendo medicación y/o prolongación de la estadía hospitalaria. Un cirujano con bajo volumen de casos fue definido como aquél que realizaba menos de 20 procedimientos por año.
> Evaluación de la cuerda vocal y seguimiento
Todos los pacientes fueron sometidos a una evaluación independiente del funcionamiento de la cuerda vocal por parte de otorrinolaringólogos que no estaban involucrados en el procedimiento quirúrgico.
Se realizó rutinariamente una laringoscopía indirecta y/o fibrolaringoscopía antes y después de la cirugía. La fibrolaringoscopía se usó en los casos en donde la visibilidad en la laringoscopía indirecta fue inadecuada o subóptima.
La laringoscopía postoperatoria se realizó antes del egreso. Se definió como una “nueva PCV”, a una PCV de comienzo nuevo diagnosticada postoperatoriamente, que no había sido detectada en el examen preoperatorio.
Los pacientes con PCV fueron programados para un control a 1 mes, y luego fueron seguidos por aproximadamente 1 año postoperatoriamente, o hasta la recuperación espontánea de la función de la cuerda vocal. La “recuperación completa” de una PCV postoperatoria fue determinada ante una recuperación total de la función normal de la cuerda vocal, documentada en el examen laringoscópico.
Una “recuperación casi completa” de la PCV fue definida como el retorno de la función de la cuerda vocal después de una parálisis, sin síntomas, con sólo una mínima disfunción residual en el examen laringoscópico. En caso de datos insuficientes del seguimiento, el resultado natural de la PCV fue definido como incierto, a menos que se hubiera verificado una lesión mayor del NLR durante la operación.
> Análisis estadístico
Todos los análisis estadísticos fueron efectuados utilizando en programa SPSS Statistics 24.0 (IBM Corp, Armonk, NY). Las variables continuas fueron expresadas como media ± desvío estándar (DE). La prueba exacta de Fisher o la de Chi-cuadrado de Pearson fueron usadas para comparar los datos nominales.
Los análisis univariados y multivariados fueron realizados sobre las variables independientes, para identificar los factores de riesgo para la PCV postoperatoria, usando modelos de regresión logística y de paso a paso con eliminación de variables. Se usó odds ratio (OR) con intervalo de confianza (IC) de 95% para reflejar la probabilidad de una nueva PCV postoperatoria.
El método de Kaplan-Meier fue empleado para estimar la tasa de recuperación de la PCV durante el seguimiento de 12 meses. Los valores de P < 0,05 fueron considerados estadísticamente significativos.
| Resultados |
Durante el período de 6 años del estudio, se efectuaron 920 operaciones tiroideas en 866 pacientes (edad media 55 ± 16 años, 82% mujeres), con 1296 nervios en riesgo.
Se efectuó la laringoscopía pre y postoperatoria en el 95% y 98% de los casos, respectivamente. Preoperatoriamente, 24 pacientes (2,8%) tenían un PCV previa a la operación primaria; 14 eran sintomáticas.
Seis habían tenido una operación tiroidea previa ipsilateral, que fue la causa probable de la lesión. Ocho pacientes con PCV preoperatoria tenían un nódulo tiroideo maligno en el mismo lado que la paresia, mientras que 10 pacientes no tuvieron una causa conocida para la PCV incidental preoperatoria, por lo que considerada idiopática. Diecinueve de las PCV preoperatorias persistieron y 5 se resolvieron durante el seguimiento después de la cirugía.
Postoperatoriamente, se detectó una nueva PCV unilateral después de 51 operaciones. Dos pacientes presentaron una nueva PCV bilateral después de la cirugía; una operación había sido realizada debido a un bocio recidivado y en la otra la indicación fue hipertiroidismo.
Dos de los 51 pacientes con una nueva PCV tenían una PCV contralateral preoperatoria y, por lo tanto, tuvieron una PCV bilateral postoperatoria. Las tasas para la nueva PCV fueron del 5,8% (n = 53/920) para las operaciones, y del 4,2% (n = 55/1296) para los nervios en riesgo.
Las tasas de nueva PCV y de PCV permanente fueron del 5,2% y 2,9% para el bocio primario, 22,5% y 15,0% para el bocio recidivado, 3,7% y 1,8% para las operaciones efectuadas por un nódulo tiroideo sospechoso, 20,5% y 12,8% para las operaciones con malignidad confirmada por BAAF, y 4,1% y 0,8% para las tiroidectomías debidas a hipertiroidismo, respectivamente. La histología maligna fue hallada en 172 (19%) de todos los 920 especímenes quirúrgicos enviados a patología.
Una enfermedad maligna no esperada fue encontrada en 39/383 (10%) de las operaciones realizadas por bocio sintomático. Las neoplasias malignas fueron confirmadas en 73/271 (27%) casos operados por nódulo tiroideo sospechoso o indeterminado.
Por otra parte, se hallaron 17 enfermedades malignas adicionales en 56 tiroidectomías para completitud (tasa de incidencia de 30% para los procedimientos para completar la resección). Cuando la BAAF reveló una sospecha alta de malignidad, el examen histológico postoperatorio confirmó el carcinoma en el 97% de los casos (uno probó ser un adenoma folicular).
> Factores de riesgo para la PCV postoperatoria
El análisis univariado de los factores de riesgo para una nueva PCV mostró que el bocio recidivado y la BAAF verificando un nódulo tiroideo maligno, fueron predictores preoperatorios prominentes de lesión el NLR durante la cirugía. Otros factores de riesgo relacionados con la operación para la lesión del NLR fueron la tiroidectomía total, disección concomitante de ganglios linfáticos, y esternotomía.
En relación con las variables postoperatorias, la hipocalcemia, histología maligna y, especialmente, enfermedad invasiva T3-T4, se asociaron con las lesiones.
Durante la operación, el cirujano identificó 722 (56%) de los 1296 nervios en riesgo. Si el NLR fue identificado como intacto, se correlacionó negativamente con el riesgo de lesión, mientras que la notificación de una posible lesión tuvo una fuerte correlación con la PCV.
Un quinto de los procedimientos fueron realizados por cirujanos con bajo volumen de casos, con una experiencia menor a 20 casos anuales (yendo desde 1 a 10 casos por año). Los cirujanos con un alto volumen de casos efectúan 20–35 operaciones por año. No obstante, no hubo una diferencia estadísticamente significativa en las tasas de PCV entre los cirujanos con bajo y alto volumen de casos: 7,1% vs 5,4% (P = 0,387).
En el análisis multivariado, los factores de riesgo significativos para la PCV fueron la tiroidectomía total, bocio recidivado, uso de drenaje e histología maligna en el examen anatomopatológico final.
Dieciocho pacientes (34%) con una nueva PCV tuvieron un factor conocido de riesgo para lesión del NLR antes de ser sometidos a cirugía (tales como cirugía previa del cuello, bocio retroesternal, o cirugía extendida requiriendo esternotomía o toracotomía).
El NLR fue sacrificado deliberadamente en 3 casos para asegurar la disección radical de un tumor maligno, y el NLR fue disecado de un tumor en 6 casos con una nueva PCV.
> Resultado natural de la PCV postoperatoria
De los 53 pacientes con una nueva PCV postoperatoria (edad media 61 ± 15 años), 42 (79%) fueron mujeres. Cuarenta y seis pacientes (87%) con una nueva PCV fueron inicialmente sintomáticos.
La recuperación completa de la PVC fue documentada con examen laringoscópico en 14 de 53 pacientes durante el seguimiento alejado. La recuperación casi completa fue clínica y visualmente documentada en 4 pacientes. Además, 4 pacientes cancelaron su visita de seguimiento porque estaban completamente asintomáticos y fueron definidos también como “recuperación casi completa”.
La PCV fue determinada definitivamente como permanente en 29 pacientes y 30 nervios en riesgo; un paciente tuvo una nueva PCV bilateral.
Dos pacientes se perdieron del seguimiento alejado a los 6 meses y, por lo tanto, su estado de recuperación fue incierto. Por esa razón, el número de PCV permanentes fue estimado entre 29 y 31 (3,2–3,4%) en 920 operaciones tiroideas, y entre 30 y 32 (2,3–2,5%) en 1296 nervios en riesgo.
Consecuentemente, la tasa estimada de recuperación completa a los 12 meses fue de 34 ± 8%, y 47 ± 8%, cuando se incluyeron las recuperaciones casi completas.
La mayoría de las recuperaciones ocurrió durante los primeros 4 meses y no ocurrió mejoría después de los 12 meses. Dos tercios de todos los pacientes con una nueva PCV recibieron terapia activa para la voz. Tres pacientes fueron sometidos a una laringoplastia con inyección de hidroxiapatita de calcio.
| Discusión |
Aunque bien reconocida y ampliamente reportada en la bibliografía, la incidencia de PCV antes y después de la cirugía tiroidea es excepcionalmente variable. Una característica importante del presente estudio fue que la decisión de detectar la PVC no descansó en el juicio del paciente o del cirujano.
En lugar de ello, prácticamente todos los casos fueron examinados independientemente por terceros investigadores (otorrinolaringólogos) con una cobertura de detección laringoscópica del 95% preoperatoriamente y del 98% postoperatoriamente.
Lang y col., argumentaron en contra del examen laringoscópico preoperatorio, basados en sus hallazgos en 302 pacientes sometidos a evaluación de la función del nervio, antes y después de la cirugía tiroidea [11].
En sus casos, la prevalencia de la PCV preoperatoria fue del 2,3% y sólo uno de los pacientes (0,4%) no había sido sometido a una cirugía tiroidea previa. Similarmente en el presente estudio, la tasa de PCV preoperatoria fue del 2,8%; no obstante, en 10 casos (1,1% de todos los pacientes), la etiología fue idiopática.
En la práctica de los autores de este trabajo, las razones para realizar una laringoscopía preoperatoria son:
(1) Para registrar, en caso de PCV postoperatoria, si de hecho era nueva y causada por el procedimiento primario
(2) En el caso de PCV preoperatoria, estar al tanto del riesgo de una PCV bilateral después de la cirugía. Hubo 2 pacientes con PCV previa unilateral que presentaron PCV bilateral después de la cirugía.
En ambos casos, la indicación para el procedimiento fue bocio recidivado y la PCV preoperatoria se debía al procedimiento primario. Afortunadamente, en ambos casos, las nuevas PCV fueron transitorias.
De acuerdo con estos resultados, la incidencia de nueva PCV fue de 53 en 920 operaciones (5,8%), y de 55 en 1296 nervios en riesgo (4,2%)
Comparado con los resultados de estudios previos en los que se usó laringoscopía de rutina [4,5], la tasa de complicaciones fue más baja (5,8% vs 7,6–13,9%). Por otro lado, se observó una tasa mucho más alta de PCV permanente que lo que había sido demostrado en esos estudios previos (3,2–3,4% vs 0,9–1,4%).
En este estudio, menos de la mitad de las PCV fueron transitorias, comparado con aproximadamente el 80%–90% en los otros estudios [4,5]. Esas diferencias remarcables necesitan ser analizadas enfocándose, por ejemplo, sobre las características de los pacientes, diagnósticos, extensión de los procedimientos quirúrgicos, estándares reportados, y volumen de casos hospitalarios y de los cirujanos.
En los hospitales que reportaron tasas más bajas de PCV permanente, las operaciones fueron realizadas generalmente por un equipo quirúrgico experimentado. La institución en donde se desempeñan los autores de este trabajo es un hospital escuela universitario y, consecuentemente, muchas operaciones son efectuadas por cirujanos en entrenamiento.
Es muy importante para cualquier institución que realiza cirugía tiroidea reconocer con certeza su tasa de lesiones del NLR, y el riesgo institucional debe ser discutido con el paciente al ponderar entre la cirugía y la vigilancia.
Los pacientes necesitan estar bien informados de las tasas de complicaciones de la institución, en lugar de brindarles sólo vagas estimaciones de los riesgos, basadas en la bibliografía.
Aunque sólo una pequeña proporción de los pacientes con PCV estuvo asintomática en este estudio (13%), la PCV postoperatoria puede ser fácilmente pasada por alto a menos que se implemente un examen rutinario de la cuerda vocal en el régimen de control de la calidad quirúrgica [2].
La visualización rutinaria del NLR es considerada como el gold standard para la prevención de su lesión [12]. En el presente estudio, la tasa de identificación del NLR fue sólo del 56%.
Interesantemente, no se halló diferencia en la tasa de PCV en los casos en los que el NLR fue visualizado, comparado con los casos en los que no lo fue. Aun así, la visualización de un NLR intacto durante la cirugía se correlacionó con una función normal de la cuerda vocal postoperatoriamente.
La evidencia de la visualización rutinaria del NLR se apoya en series de casos, tales como la reciente publicación de Dhillon y col., del John Hopkins Hospital, que incluyó 2527 nervios en riesgo, con evaluación rutinaria del NLR por el cirujano actuante en todos los casos; las tasas reportadas de PCV temporaria (2,9%) y permanente (0,4%) para los nervios en riesgo, fueron significativamente más bajas que las del presente estudio [13].
No obstante, el estudio de esos autores tuvo una cohorte mixta, incluyendo procedimientos sobre paratiroides, mientras que los procedimientos repetidos no fueron incluidos; la tasa postoperatoria de PCV fue de 72/2153 nervios en riesgo (3,3%) en los procedimientos tiroideos primarios, comparada con 55/1296 (4,2%) en este estudio, con procedimientos tanto primarios como repetidos.
Asimismo, el estudio de Dhillon representa la vasta experiencia de un único cirujano con alto volumen de casos, en uno de los hospitales mundialmente más renombrados, mientras que el presente estudio es una representación en el “mundo real” de los resultados en un hospital pequeño.
Durante el período del estudio, no se usó el neuromonitoreo intraoperatorio. Aunque es ampliamente recomendado en situaciones especiales, tales como la cirugía repetida, de acuerdo con 2 meta-análisis con 23.500 y 9000 pacientes agrupados, el uso rutinario del neuromonitoreo no mostró el descenso de las tasas de PCV [12,14].
Considerando la alta tasa de PCV permanente en el presente estudio, los autores modificaron su técnica después del mismo, para incluir el neuromonitoreo y recomiendan la identificación rutinaria del NLR.
El presente estudio confirmó que el bocio recidivado en uno de los factores de riesgo más significativos para la PCV postoperatoria, con un riesgo casi nueve veces mayor que todos los otros indicadores combinados.
Previamente, se había visto que los pacientes con bocio benigno recidivado tenían un riesgo 4,7 veces mayor de PCV permanente en un estudio multi-institucional con 16.448 procedimientos [6]. Mientras que ese riesgo está bien identificado en la bibliografía, puede estar aún subestimado en el trabajo clínico. Los beneficios de la repetición de la cirugía deben ser cuidadosamente ponderados contra el riesgo de lesión del NLR.
Otros factores de riesgo para la lesión del NLR en este estudio fueron la tiroidectomía total, esternotomía, disección de ganglios linfáticos, hipocalcemia y uso de drenaje. En la tiroidectomía total, ambos NLR estuvieron en riesgo y, por lo tanto, el riesgo fue al menos dos veces mayor comparado con la hemitiroidectomía.
La esternotomía, disección de ganglios linfáticos, hipocalcemia y uso de drenaje (en sólo el 6% de las operaciones), estuvieron todos relacionados con una cirugía extensa y, por lo tanto, con un mayor riesgo de lesión del NLR. El uso de drenaje en sí mismo no ha sido identificado como un factor de riesgo para la PCV en un meta-análisis con 1927 pacientes [15].
En el presente estudio, el drenaje fue utilizado más liberalmente, en el 51% de los pacientes. Este trabajo fue realizado en un momento en donde el uso de dispositivos de energía (esto es, instrumentos de sellado electrónico) había sido adaptado a la práctica de rutina (usado en el 99% de los casos).
El efecto de los dispositivos de energía en la tasa de lesiones del NLR no pudo ser evaluado, porque no hubo suficientes casos para un grupo control; sólo unos pocos pacientes fueron operados sin el instrumento para el sellado de vasos.
Casi idénticamente a un meta-análisis previo de 1798 pacientes, dos tercios de los pacientes con PCV en el presente estudio recibieron terapia vocal, mientras que sólo el 5,7% fue sometido a laringoplastia con inyección [16]. La terapia temprana de la voz en pacientes con PCV unilateral se ha asociado con mejores resultados que la rehabilitación tardía, en un estudio retrospectivo de 11 años con 171 pacientes [17].
La laringoscopía de rutina postoperatoria permite el diagnóstico temprano y, en consecuencia, la iniciación de la terapia vocal sin retraso, lo que también es importante para la prevención de los problemas relacionados con la aspiración.
Asimismo, la detección rutinaria de la cuerda vocal brinda una retroalimentación directa al cirujano y puede ayudar a evitar las lesiones del NLR en el futuro.
> Limitaciones del estudio
Aunque este estudio observacional fue efectuado prospectivamente, el seguimiento alejado no estuvo estructurado y los datos del mismo fueron extraídos de manera retrospectiva. Unos pocos pacientes con PCV declinaron el seguimiento a 12 meses y, por lo tanto, se utilizó el método de Kaplan-Meier con cesura de datos para estimar la tasa de recuperación.
No fue claramente definido si el NLR fue identificado antes o después de la remoción del lóbulo tiroideo. En consecuencia, los resultados relacionados con la identificación del NLR deben ser interpretados con cautela.
Conclusiones
- Este estudio resalta el significado de la detección rutinaria de la PCV en la cirugía tiroidea.
- Casi el 3% de los pacientes tuvo incidentalmente una PCV preoperatoria, que pudo ser verificada sólo con la laringoscopía preoperatoria efectuada rutinariamente.
- El riesgo de una PCV postoperatoria de nuevo comienzo fue mayor entre los pacientes con bocio recidivado y patología maligna tiroidea (especialmente en estadios T3-T4).
- Esos grupos de pacientes necesitan ser bien informados del riesgo aumentado antes de la cirugía.
- Menos de la mitad de las PCV se resolvieron completamente en el postoperatorio, lo que brindó una tasa marcadamente inferior que la reportada previamente.
Referencias bibliográficas
- Jeannon JP, Orabi AA, Bruch GA, Abdalsalam HA, Simo R (2009) Diagnosis of recurrent laryngeal nerve palsy after thyroidectomy: a systematic review. Int J Clin Pract 63:624–629
- Bergenfelz A, Jansson S, Kristoffersson A et al (2008) Complications to thyroid surgery: results as reported in a database from a multicenter audit comprising 3,660 patients. Langenbecks Arch Surg 393:667–673
- Stager SV (2014) Vocal fold paresis: etiology, clinical diagnosis and clinical management. Curr Opin Otolaryngol Head Neck Surg 22:444–449
- Lo CY, Kwok KF, Yuen PW (2000) A prospective evaluation of recurrent laryngeal nerve paralysis during thyroidectomy. Arch Surg 135:204–207
- Joliat GR, Guarnero V, Demartines N, Schweizer V, Matter M (2017) Recurrent laryngeal nerve injury after thyroid and parathyroid surgery: incidence and postoperative evolution assessment. Medicine (Baltimore) 96:e6674
- Dralle H, Sekulla C, Haerting J et al (2004) Risk factors of paralysis and functional outcome after recurrent laryngeal nerve monitoring in thyroid surgery. Surgery 136:1310–1322
- Erbil Y, Barbaros U, Issever H et al (2007) Predictive factors for recurrent laryngeal nerve palsy and hypoparathyroidism after thyroid surgery. Clin Otolaryngol 32:32–37
- Enomoto K, Uchino S, Watanabe S, Enomoto Y, Noguchi S (2014) Recurrent laryngeal nerve palsy during surgery for benign thyroid diseases: risk factors and outcome analysis. Surgery 155:522–528
- Haugen BR, Alexander EK, Bible KC et al (2016) 2015 American thyroid association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer: the American Thyroid Association guidelines task force on thyroid nodules and differentiated thyroid cancer. Thyroid 26:1–133
- Cibas ES, Ali SZ (2009) The bethesda system for reporting thyroid cytopathology. Thyroid 19:1159–1165
- Lang BH, Chu KK, Tsang RK, Wong KP, Wong BY (2014) Evaluating the incidence, clinical significance and predictors for vocal cord palsy and incidental laryngopharyngeal conditions before elective thyroidectomy: Is there a case for routine laryngoscopic examination? World J Surg 38:385–391.
- Pisanu A, Porceddu G, Podda M, Cois A, Uccheddu A (2014) Systematic review with meta-analysis of studies comparing intraoperative neuromonitoring of recurrent laryngeal nerves versus visualization alone during thyroidectomy. J Surg Res 188:152–161
- Dhillon VK, Rettig E, Noureldine SI et al (2018) The incidence of vocal fold motion impairment after primary thyroid and parathyroid surgery for a single high-volume academic surgeon determined by pre- and immediate post-operative fiberoptic laryngoscopy. Int J Surg 56:73–78¿
- Yang S, Zhou L, Lu Z, Ma B, Ji Q, Wang Y (2017) Systematic review with meta-analysis of intraoperative neuromonitoring during thyroidectomy. Int J Surg 39:104–113
- Tian J, Li L, Liu P, Wang X (2017) Comparison of drain versus no-drain thyroidectomy: a meta-analysis. Eur Arch Otorhinolaryngol 274:567–577
- Chen X, Wan P, Yu Y et al (2014) Types and timing of therapy for vocal fold paresis/paralysis after thyroidectomy: a systematic review and meta-analysis. J Voice 28:799–808
- Mattioli F, Menichetti M, Bergamini G et al (2015) Results of early versus intermediate or delayed voice therapy in patients with unilateral vocal fold paralysis: our experience in 171 patients. J Voice 29:455–458