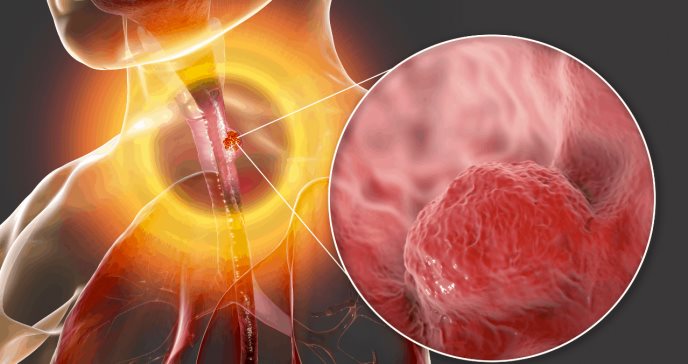
El cáncer de esófago (CE) es la sexta causa más común de muerte asociada al cáncer en todo el mundo, lo que representa aproximadamente 1 de cada 20 muertes por cáncer.
A nivel mundial, el tipo más común de CE es el carcinoma de células escamosas, seguido del adenocarcinoma, mientras que el carcinoma de células pequeñas, el melanoma, el sarcoma y el linfoma son raros. Sin embargo, en los países occidentales, el adenocarcinoma esofágico (AdE) es mucho más común que el carcinoma de células escamosas del esófago, y su incidencia está aumentando rápidamente en los países desarrollados, debido en parte a la creciente prevalencia de la obesidad y la enfermedad por reflujo gastroesofágico.
El AdE tiene un pronóstico favorable si se diagnostica precozmente, cuando toda vía no ha alcanzado las capas mucosa y submucosa del esófago. Sin embargo, es lamentable que la mayoría de los casos se diagnostican en una etapa tardía, cuando ya el pronóstico es sombrío. La tasa de supervivencia general a 5 años de pacientes con AdE es <20 %, comparable a la de los pacientes que tienen cáncer de hígado, pulmón o páncreas. Por lo tanto, existe una necesidad imperiosa de estrategias de tamizaje efectivas para el diagnóstico precoz.
El tratamiento se ha centrado principalmente en la resección, ya sea quirúrgica o, más recientemente, endoscópica. Históricamente, la radioterapia y la quimioterapia han sido aplicadas cunando la resección es menos factible debido a que el cáncer ya se ha propagado. Para el CE en general, el abordaje multidisciplinario puede ayudar a identificar cuál es la mejor estrategia terapéutica en función de las características del paciente y del tumor, además de la experiencia local.
| Factores de Riesgo |
> Obesidad
Un metanálisis de más de 16.000 casos confirmó una estrecha asociación entre el índice de masa corporal, la obesidad y el AdE.
> Factores de riesgo múltiples
En otro estudio se halló que la prevalencia del esófago de Barrett (lesión precursora del AdE) tenía una relación lineal positiva con el número de factores de riesgo, como la enfermedad gastroesofágica por reflujo, el sexo masculino, la edad >50 años, los antecedentes familiares de esófago de Barrett o AdE y, la obesidad (definida por un índice de masa corporal >35 kg/m2).
> Otros factores poco fiables
Síntomas. La mayoría de los pacientes con AdE en etapa temprana son >65 años y son asintomáticos. Debido a su distensibilidad, el esófago puede disimular tumores más pequeños que permanecen asintomáticos hasta que la lesión crece a un tamaño significativo. Dado que la enfermedad por reflujo gastroesofágico afecta principalmente al esófago distal y la unión gastroesofágica, el 94 % de los cánceres asociados con el esófago de Barrett se encuentran pasando la bifurcación traqueal.
La disfagia significativa asociada a lesiones tempranas debe despertar la sospecha de enfermedad más avanzada o, rara vez, de una causa no maligna concurrente como la estenosis péptica, la inflamación o el tumor submucoso concurrente.
La esofagitis eosinofílica causa inflamación crónica del esófago, lo que plantea la duda acerca de si puede aumentar la transformación maligna. Sin embargo, un estudio con una gran base de datos reciente no pudo hallar una relación entre la esofagitis eosinofílica y el CE.
El consumo de alcohol no parece aumentar el riesgo de AdE, y algunos estudios sugieren que el vino puede ser protector.
| ¿Quién se debe examinar? |
Se cree que el esófago de Barrett es el principal precursor del AdE, ya que progresa a través de etapas patológicasꟷmetaplasia a displasia de bajo grado, luego displasia de alto grado hasta llegar al AdE.
El aumento del AdE y su mal pronóstico en las etapas avanzadas han aumentado el interés en la detección del esófago de Barrett y su estrecho seguimiento. En un estudio prospectivo, los casos de CE en pacientes con esófago de Barrett que fueron sometidos a vigilancia endoscópica fueron diagnosticados en una etapa más temprana que en la población general. Sin embargo, los estudios no han logrado identificar una herramienta precisa, rentable y ampliamente aplicable que pueda reducir la tasa de mortalidad.
Las guías actuales, basadas en evidencia de baja calidad y opinión de expertos, restringen la detección a una población de pacientes muy específica. Es decir, aquellos con enfermedad por reflujo gastroesofágico de larga data (>5 años) y aquellos con síntomas frecuentes de reflujo (semanalmente o más) con ≥2 factores de riesgo de esófago de Barrett o AdE.
Estos factores de riesgo incluyen sexo masculino, edad >50 años, obesidad central (perímetro de cintura >102 cm o relación cintura-cadera >0,9), antecedentes de tabaquismo pasado o presente, raza blanca, antecedentes familiares de primer grado de esófago de Barrett o AdE o, hernia hiatal.
Los pacientes con diagnóstico de esófago de Barrett sin displasia deben someterse a una endoscopia cada 3 a 5 años. En un gran estudio a nivel nacional, el riesgo anual de AdE a partir del diagnóstico de esófago de Barrett fue de 0,12%, muy inferior al riesgo asumido del 0,5%, que consideran las guías actuales.
Sin embargo, casi el 90% de los casos de AdE se diagnostican en pacientes en quienes se desconoce la existencia del esófago de Barrett. Esto demuestra que las pautas de detección actuales continúan sin ser cumplidas en un gran número de pacientes en riesgo.
La endoscopía superior es el estándar de oro para la detección, pero requiere sedación y es relativamente costosa e inconveniente como procedimiento de detección. Una herramienta de detección ideal debe ser relativamente económica, bien tolerada y aplicable en la práctica general.
Las tasas de detección del esófago de Barrett han mejorado con los avances de la endoscopía, como las imágenes de alta definición, la cromoendoscopía (que utiliza una tinción especial para mejorar la visualización de la mucosa) y la proyección de imagen de banda estrecha (que mejora la visualización de la mucosa con resolución basada en la selección longitudes de onda específicas de luz).
Los estudios de deglución, como la deglución de bario no permiten evaluar la histología de la metaplasia o la displasia. Por lo tanto, no deben ser utilizadas para la detección o vigilancia del esófago de Barrett.
| Nuevos métodos de detección para el esófago de Barrett |
Actualmente están en investigación métodos que no requieren endoscopia con sedación.
> La citoesponja es una cápsula para ingerir que contiene una esponja adherida a una cuerda. La cápsula se disuelve al alcanzar el estómago y suelta la esponja, que puede ser retirada del esófago a través de la boca tirando de la cuerda. En su salida por el esófago, la esponja recoge las células epiteliales las que luego se analizan en busca de biomarcadores del esófago de Barrett , como el factor Trébol 3. La citoesponja es económica y segura. Un estudio prospectivo halló que tiene una sensibilidad del 73% y una especificidad del 94% para detectar lesiones de al menos 1 cm, resultados que se repitieron en una revisión sistemática. De manera similar, un dispositivo de globo deglutido puede tomar muestras del esófago distal y detectar marcadores de metilación del ADN. Su sensibilidad para la detección de metaplasia del esófago de Barrett fue del 90,3% y su especificidad del 91,7%.
> La endoscopia transnasal, otra técnica aplicable en el consultorio, utiliza un endoscopio reutilizable con una vaina estéril exterior desechable. Parece ser mejor tolerada que la endoscopia estándar y sus hallazgos son similares.
> La prueba del aliento utiliza una “nariz electrónica” para detectar compuestos orgánicos volátiles en el aire exhalado y ha mostrado resultados prometedores, con una sensibilidad del 91% y una especificidad del 74%.
Estas nuevas herramientas de detección pueden ser eficientes y rentables en atención primaria. Sin embargo, se necesita más investigación antes de que puedan ser ampliamente adoptadas. Se están realizando ensayos clínicos para evaluar la aceptación y la preferencia de los pacientes respecto de estas diferentes herramientas.
| Medidas preventivas posibles |
Aunque los estudios epidemiológicos sugirieron que la aspirina y los antiinflamatorios no esteroideos podrían prevenir el esófago de Barrett y el AdE,, en los ensayos clínicos estos fármacos no han tenido éxito.
| Dietas |
Datos retrospectivos de muchos centros muestran que las dietas ricas en antioxidantes, frutas, verduras, ácidos grasos omega-3, grasas poliinsaturadas y fibra se asocian con menor riesgo de esófago de Barrett.
| La biopsia es el estándar de oro para el diagnóstico |
En la endoscopía, las lesiones tempranas del AdE pueden ser planas, polipoides o levemente deprimidas. Los tumores avanzados se presentan como masas que pueden obstruir la luz esofágica. El estándar de oro para el diagnóstico de AdE es el muestreo de tejido por biopsia endoscópica. Un ensayo prospectivo reveló una precisión diagnóstica del 93% con una sola biopsia; con muestras de biopsia adicionales el rendimiento aumentó a >98%.
| La estadificación del cáncer es fundamental |
Una vez que el AdE es diagnosticado, se debe evaluar su estadio para determinar el pronóstico y el tratamiento. Esto involucra el sistema TNM de la siguiente manera:
• Profundidad del tumor (categorizado en la escala de Tis como T4b)
• Ganglios, es decir, número de ganglios linfáticos afectados (clasificados en una escala de N0 a N3)
• Metástasis en órganos distantes (M0 para no metástasis a distancia o M1 para metástasis a distancia).
> Tomografía por emisión de positrones con tomografía computarizada. El papel de la tomografía por emisión de positrones con 18-fluorodesoxiglucosa (FDG) con tomografía computarizada (PET/TC) y de la ecografía endoscópica en los primeros estadios del AdE es controvertido. Sin embargo, para evaluar la diseminación nodal en casos de cáncer avanzado (≥T1b) las pautas de la guía de la National Comprehensive Cancer Network (Red Nacional Integral del Cáncer) recomienda la estadificación por PET/TC y la ecografía endoscópica. La PET/TC es menos beneficiosa en casos de AdE temprano que en la enfermedad avanzada. Algunos estudios hallaron que no podía detectar de manera confiable los estadios tempranos de ese cáncer, como tumores T1a y T1b.
Un estudio de 79 pacientes con estadificación clínica de AdE T1a y T1b sometidos a una PET/TC preoperatoria mostró que todos los ganglios ávidos de FDG observados fueron positivos falsos; otro estudio tuvo hallazgos similares. Esto sugiere que la PET/TC podría dar lugar a la realización de más biopsias innecesarias. No obstante, si se encuentra un tumor más avanzado en el estudio patológico posterior a la disección submucosa endoscópica, la PET/TC después de la resección tiene una utilidad limitada, ya que la inflamación del lecho de resección suele ser ávida de FDG en la PET. Por lo tanto, se considera la PET/TC antes de la resección de tumores voluminosos o borderline mayores de 15 mm o lesiones con sospecha de invasión superficial (SM1) >500 micras.
La ecografía endoscópica puede evaluar la profundidad de la invasión tumoral y la diseminación de los ganglios linfáticos locorregionales. Sin embargo, tiene una tasa elevada de positivos falsos de hasta el 10%. En consecuencia, las guías de la American Society for Gastrointestinal Endoscopy desaconseja su uso rutinario para el AdE a estadio mucoso (T1a) y la enfermedad submucosa (T1b).
En la actualidad, los tumores más avanzados son tratados con resección endoscópica. De este modo, antes de proceder con el tratamiento endoscópico es primordial estadificar de manera precisa y descartar la enfermedad avanzada. Se requiere más investigación para comprender el papel de PET/TC y la ecografía endoscópica en tumores grandes (>15 mm) T1a y la enfermedad temprana T1b, cada vez más para la resección endoscópica.
Opciones de tratamiento
> Cirugía
Durante décadas, el tratamiento de primera línea para el AdE, incluido el esófago de Barrett, ha sido la resección quirúrgica abierta. Los avances técnicos en cirugía, como la esofagectomía mínimamente invasiva asistida por robot, la esofagectomía mínimamente invasiva y las imágenes tridimensionales han mejorado los tiempos de recuperación y la identificación y exéresis de los ganglios linfáticos, habiendo disminuido significativamente el dolor posoperatorio, el sangrado intraoperatorio y la duración de la estancia hospitalaria.
Los enfoques mínimamente invasivos se han convertido en los preferidos, con resultados a largo plazo no inferiores a los de la esofagectomía abierta, con una mortalidad a los 90 días de casi 7 %, similar a la de todos los abordajes quirúrgicos. Sin embargo, las tasas de mortalidad fueron más bajas para los pacientes con tumores T1a (3,1%) y tumores T1b (6,0%).
El papel de la esofagectomía quirúrgica sigue siendo controvertido en los tumores T1a tempranos con características de alto riesgo, como la escasa diferenciación y el gran tamaño, debido a las tasas elevadas de mortalidad perioperatoria (3%-6%) y morbilidad, con un riesgo similar de diseminación locorregional (4,2%).
Sin embargo, la esofagectomía inmediata sigue siendo indicada para los tumores T1b en personas por lo demás sanas debido al mayor riesgo de metástasis en los ganglios linfáticos (22%–28%). También se comprobaron mayores tasas de supervivencia general y remisión histológica en comparación con la resección endoscópica. Sin embargo, los pacientes tratados endoscópicamente eran mayores y tenían múltiples comorbilidades.
Las complicaciones quirúrgicas posoperatorias afectan las tasas de mortalidad a largo plazo. Las complicaciones específicas del procedimiento incluyen anomalías del conducto y lesión del nervio laríngeo recurrente; las complicaciones sistémicas incluyen fibrilación auricular, infarto de miocardio y neumonía.
Las secuelas a largo plazo de la esofagectomía incluyen trastornos funcionales como disfagia, retardo del vaciado gástrico, reflujo y síndrome de vaciamiento gástrico. Sin embargo, la esofagectomía suele ser bien tolerada a largo plazo, con cambios en el estilo de vida tales como comer porciones de comidas pequeñas y frecuentes, lentamente, evitando los alimentos y las bebidas con elevado contenido de azúcar.
> Cirugía endoscópica
Las modernas técnicas y dispositivos endoscópicos condujeron a un cambio hacia el tratamiento endoscópico del CE reemplazando a la cirugía, aunque no todos los AdE tempranos son susceptible de resección endoscópica curativa.
La arquitectura esofágica tiene la característica de que los linfáticos penetran a través de la muscularis mucosa y llegan a la lámina propia, lo que crea un riesgo teórico de metástasis en los ganglios linfáticos de los tumores tempranos (T1a).
Se cree que en el cáncer relacionado con el esófago de Barrett, la mucosa tiene un riesgo pequeño (1%–2%) de metástasis en los ganglios linfáticos, que aumenta con la invasión más profunda de la submucosa:
• 7,5% con invasión submucosa superficial
• 10% con la invasión en el tercio medio de la submucosa
• 45% con la invasión submucosa profunda.
La resección endoscópica puede ser considerada en tumores con bajo riesgo de metástasis en los ganglios linfáticos o en tumores de alto riesgo en pacientes que no son médicamente aptos para la cirugía. Los riesgos de muerte perioperatoria y de diseminación regional son 3% y 4%. Por lo tanto, antes de decidir cuál es el mejor enfoque terapéutico para el AdE temprano es importante sopesar el riesgo de metástasis en los ganglios linfáticos y el riesgo de morbilidad y mortalidad de la cirugía. Hay 2 técnicas de resección endoscópica principales: la resección mucosa endoscópica y la disección submucosa endoscópica.
La resección endoscópica de la mucosa se puede realizar mediante 2 métodos principales: de resección endoscópica de la mucosa asistida por capuchón, en la que se adjunta una tapa a la punta del endoscopio para deprimir los pliegues de la mucosa y permitir una mejor visualización y bandeo. La resección de la mucosa endoscópica esofágica presenta un riesgo del 1,2% de sangrado, 1% de riesgo de formación de estenosis y bajo riesgo de perforación (0,2%-1,3%). La seguridad, las tasas de éxito y la facilidad de procedimiento de la resección endoscópica de la mucosa han permitido que se establezca como un pilar en el tratamiento del AdE temprano. Sin embargo, para las lesiones más grandes, este procedimiento requiere extirpar el tumor en múltiples piezas, lo que se asocia con mayores tasas de recurrencia.
La disección submucosa endoscópica puede permitir la extirpación de tumores aún más grandes en una sola pieza (en bloque) y se asocia con mayores tasas de curación y menor riesgo de recurrencia, permitiendo además, un análisis histopatológico preciso. Un ensayo prospectivo que comparó las resecciones mucosa y submucosa endoscópica con la disección para el tratamiento del esófago de Barrett y el AdE halló que la tasa de resección en bloque fue del 100 % con la disección submucosa endoscópica, pero solo del 15 % con la resección mucosa endoscópica. Asimismo, un metanálisis mostró mayores tasas de resección R0 (márgenes libres de neoplasia) (92,3% vs. 52,7%) y menores tasas de recurrencia local (0,3% vs. 11,5%) con la disección submucosa endoscópica que con resección mucosa endoscópica.
> Quimiorradiación
El AdE temprano (T1a, T1b) se maneja principalmente mediante la resección endoscópica o la cirugía. Sin embargo, la evidencia reciente sugiere que puede haber un papel para la terapia neoadyuvante (antes de la resección) o la quimiorradioterapia adyuvante (después de la resección) en la enfermedad temprana, particularmente en pacientes con tumores de alto riesgo (resección incompleta, márgenes profundos positivos, invasión linfovascular, tumores escasamente diferenciados, tumores >2 cm) que son médicamente no apto para la cirugía con disección de ganglios linfáticos.
El ChemoRadiotherapy for Oesophageal Cancer Followed by Surgery Study incluyó a pacientes con AdE resecable T1 a T3 y N0 a N1 y mostró mayores tasas de supervivencia cuando los pacientes fueron sometidos a quimiorradioterapia neoadyuvante antes de la cirugía. Cabe señalar que los datos sobre este tema son limitados porque los estudios que incluyeron solo a pacientes con carcinoma de células escamosas del esófago.
El paclitaxel y el carboplatino comúnmente son utilizados con radioterapia concurrente. Otra combinación que se utiliza cada vez más es 5-fluorouracilo y oxaliplatino junto con la radioterapia. Un ensayo aleatorizado en curso está comparando estos 2 regímenes adyuvantes para el AdE resecable.
La radioterapia sola (haz externo o braquiterapia) puede ser una opción para los pacientes >65 años con AdE que no pueden ser sometidos a cirugía o terapia endoscópica y quimioterapia concurrentes. Los datos sobre tratamiento de radiación solo provienen principalmente de series retrospectivas en pacientes con CE de células escamosas.
Los candidatos quirúrgicos deficientes que reciben un tratamiento definitivo con quimiorradioterapia pueden tener lesiones residuales, recurrentes y o enfermedad metacrónica. Estos pacientes pueden ser manejados con terapia de rescate mediante disección submucosa endoscópica o ablación. Se necesitan más estudios para explorar la utilidad de la quimiorradiación neoadyuvante o adyuvante para el tratamiento del AdE temprano.
| Tratamiento adyuvante después de tratamiento con resección endoscópica no curativo |
Los pacientes con AdE temprano se tratan cada vez más con resección endoscópica. Sin embargo, algunas resecciones no son curativas, con poca diferenciación, invasión linfovascular, invasión submucosa profunda o márgenes positivos. Estos pacientes son de mayor riesgo de metástasis en los ganglios linfáticos y enfermedad progresiva.
Idealmente, para estos pacientes, el tratamiento de elección es la esofagectomía con o sin quimiorradioterapia adyuvante. Sin embargo, los pacientes con características de alto riesgo después de la resección endoscópica y que son malos candidatos para la esofagectomía definitiva con la disección de los ganglios linfáticos pueden ser sometidos a la quimiorradioterapia.
Un ensayo prospectivo en pacientes con carcinoma de células escamosas de esófago T1a que fueron sometidos a la disección submucosa endoscópica halló una tasa de supervivencia libre de recurrencia a los 3 años del 100 % en aquellos que recibieron radioterapia adyuvante y del 85,3 % en quienes no la recibieron. Se destaca que no se noto la existencia de eventos adversos graves por efecto de la radiación.
| Vigilancia después de la resección endoscopia curativa |
En el AdE, la resección endoscópica se considera curativa si la histología muestra “bien diferenciada a moderadamente diferenciado”, sin invasión de los ganglios linfáticos, con menos de 500 μm de invasión submucosa combinada con márgenes laterales y profundos negativos.
En comparación, para el carcinoma de células escamosas, los criterios de resección curativa endoscópica incluyen la resección en bloque R0 de lesiones superficiales que invaden la lámina propia (T1a m2) con histología “bien diferenciado a moderadamente diferenciado” sin invasión linfovascular. La resección R0 en bloque de un tumor bien diferenciado m3 o sm1 (<200 μm) sin invasión linfovascular, tiene un riesgo bajo de metástasis en los ganglios linfáticos; estos características son una indicación relativa de disección submucosa endoscópica.
Los pacientes que se someten a una resección endoscópica completa del esófago de Barrett o del AdE están inscritos en un programa de vigilancia posterior al tratamiento. La vigilancia postoperatoria se estratifica según la estadificación patológica posterior a la resección:
Para esófago de Barrett con alto grado displasia, se hará una endoscopia superior cada 6 meses durante 2 años, a partir de los cuales, se recomienda hacerla anualmente.
Para el AdE T1a, pueden ser útiles la ecografía endoscópica y la TC, ya que estas lesiones tienen un 1% a 2% de riesgo de metástasis en los ganglios linfáticos. La vigilancia consiste en hacer ecografías endoscópicas cada 6 meses durante 2 años, luego ecografía endoscópica anual y TC de tórax y abdomen, anualmente durante 5 años.
Para las resecciones de alto riesgo, la vigilancia incluye ecografía endoscópica cada 3 meses durante el primer año, luego cada 6 meses durante 1 año y luego anualmente. La TC de tórax y abdomen se recomienda a menores intervalos: cada 6 meses durante el primer año y anual durante los 5 años siguientes.
| Resultado final |
El AdE temprano se diagnostica comúnmente por casualidad en pacientes sin síntomas que son sometidos a una endoscopía superior por otras razones.
Debido a la anatomía única del esófago, incluso el AdE temprano tiene un riesgo de metástasis en los ganglios linfáticos, y es necesario un manejo adecuado.
Para las lesiones pequeñas de AdE (<1,5 cm), muchos estudios han demostrado que la resección endoscópica de la mucosa es una estrategia eficaz con buenos resultados a largo plazo. Para las lesiones más grandes o sospecha de invasión más profunda o carcinoma de células escamosas, se justifica un enfoque multidisciplinario.
La disección submucosa endoscópica puede ser utilizada con eficacia para extirpar tumores superficiales, a pesar de su tamaño o fibrosis asociada. Sin embargo, para las lesiones que involucran más de dos tercios de la circunferencia del esófago, existe el riesgo de estenosis esofágica.
Los pacientes con AdE temprano y riesgo de metástasis en los ganglios linfáticos se tratan mejor con resección quirúrgica, la que permite la disección de los ganglios linfáticos, pero muchos pacientes >65 años o aquellos con comorbilidades importantes pueden no ser candidatos para la cirugía.
En estos pacientes puede ser útil la resección endoscópica con quimioterapia o radioterapia adyuvante. Algunos pacientes con AdE temprano pueden no ser candidatos para la resección endoscópica o quirúrgica debido a la invasión profunda de la submucosa, enfermedad cicatrizada, radioterapia del campo previa, o comorbilidades graves que impidan la anestesia para el procedimiento. En estos pacientes se puede realizar la radioterapia neoadyuvante, braquiterapia, quimioterapia o una combinación de éstos.
REFERENCIAS:
1. Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018; 68(6):394–424. doi:10.3322/caac.21492.
2. National Cancer Institute. Surveillance, Epidemiology, and End Results Program. SEER* Explorer: an interactive website for SEER cancer statistics. https://seer.cancer.gov. Accessed April 22, 2022.
3. Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020. CA Cancer J Clin 2020; 70(1):7–30. doi:10.3322/caac.21590.
4. Tian J, Zuo C, Liu G, et al. Cumulative evidence for the relationship between body mass index and the risk of esophageal cancer: an updated meta-analysis with evidence from 25 observational studies. J Gastroenterol Hepatol 2020; 35(5):730–743. doi:10.1111/jgh.14917
5. Qumseya BJ, Bukannan A, Gendy S, et al. Systematic review and meta-analysis of prevalence and risk factors for Barrett’s esophagus. Gastrointest Endosc 2019; 90(5):707–717.e1. doi:10.1016/j.gie.2019.05.030
6. Syed A, Maradey-Romero C, Fass R. The relationship between eosinophilic esophagitis and esophageal cancer. Dis Esophagus 2017; 30(7):1–5. doi:10.1093/dote/dox050
7. Anderson LA, Cantwell MM, Watson RG, et al. The association between alcohol and refl ux esophagitis, Barrett’s esophagus, and esophageal adenocarcinoma. Gastroenterology 2009; 136(3): 799–805 doi:10.1053/j.gastro.2008.12.005
8. Codipilly DC, Chandar AK, Singh S, et al. The effect of endoscopic surveillance in patients with Barrett’s esophagus: a systematic review and meta-analysis. Gastroenterology 2018; 154(8):2068-2086.e5. doi:10.1053/j.gastro.2018.02.022
9. Kastelein F, van Olphen SH, Steyerberg EW, Spaander MC, Bruno MJ; ProBar-Study Group. Impact of surveillance for Barrett’s oesophagus on tumour stage and survival of patients with neoplastic progression. Gut 2016; 65(4):548–554. doi:10.1136/gutjnl-2014-308802
10. ASGE Standards of Practice Committee, Qumseya B, Sultan S, Bain P, et al. ASGE guideline on screening and surveillance of Barrett’s esophagus. Gastrointest Endosc 2019; 90(3):335–359.e2. doi:10.1016/j.gie.2019.05.012
11. Hvid-Jensen F, Pedersen L, Drewes AM, Sørensen HT, Funch-Jensen P. Incidence of adenocarcinoma among patients with Barrett’s esophagus. N Engl J Med 2011; 365(15):1375–1383. doi:10.1056/NEJMoa1103042
12. Tan MC, Mansour N, White DL, Sisson A, El-Serag HB, Thrift AP. Systematic review with meta-analysis: prevalence of prior and concurrent Barrett’s oesophagus in oesophageal adenocarcinoma patients. Aliment Pharmacol Ther 2020; 52(1):20–36. doi:10.1111/apt.15760
13. Kadri SR, Lao-Sirieix P, O’Donovan M, et al. Acceptability and accuracy of a non-endoscopic screening test for Barrett’s esophagus in primary care: cohort study. BMJ 2010; 341:c4372. doi:10.1136/bmj.c4372
14. Iqbal U, Siddique O, Ovalle A, Anwar H, Moss SF. Safety and effi cacy of a minimally invasive cell sampling device (‘Cytosponge’) in the diagnosis of esophageal pathology: a systematic review. Eur J Gastroenterol Hepatol 2018; 30(11):1261–1269. doi:10.1097/MEG.0000000000001210
15. Moinova HR, LaFramboise T, Lutterbaugh JD, et al. Identifying DNA methylation biomarkers for non-endoscopic detection of Barrett’s esophagus. Sci Transl Med 2018; 10(424):eaao5848. doi:10.1126/scitranslmed.aao5848
16. Shariff MK, Varghese S, O’Donovan M, et al. Pilot randomized crossover study comparing the effi cacy of transnasal disposable endosheath with standard endoscopy to detect Barrett’s esophagus. Endoscopy 2016; 48(2):110–116. doi:10.1055/s-0034-1393310
17. Peters Y, Schrauwen RWM, Tan AC, Bogers SK, de Jon B, Siersema PD. Detection of Barrett’s oesophagus through exhaled breath using an electronic nose device. Gut 2020; 69(7):1169–1172. doi:10.1136/gutjnl-2019-320273
18. Heath EI, Canto MI, Piantadosi S, et al. Secondary chemoprevention of Barrett’s esophagus with celecoxib: results of a randomized trial. J Natl Cancer Inst 2007; 99(7):545–557. doi:10.1093/jnci/djk112
19. Kubo A, Levin TR, Block G, et al. Dietary antioxidants, fruits, and vegetables and the risk of Barrett’s esophagus. Am J Gastroenterol 2008; 103(7):1614–1624. doi:10.1111/j.1572-0241.2008.01838.x
20. Kubo A, Block G, Quesenberry CP Jr, Buffl er P, Corley DA. Effects of dietary fi ber, fats, and meat intakes on the risk of Barrett’s esophagus. Nutr Cancer 2009; 61(5):607–616. doi:10.1080/01635580902846585
21. Graham DY, Schwartz JT, Cain GD, Gyorkey F. Prospective evaluation of biopsy number in the diagnosis of esophageal and gastric carcinoma. Gastroenterology 1982; 82(2):228–231. pmid:7054024
22. Ajani JA, D’Amico TA, Bentrem DJ, et al. Esophageal and esophagogastric junction cancers, version 2.2019, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw 2019; 17(7):855– 883. doi:10.6004/jnccn.2019.0033
23. Cuellar SL, Carter BW, Macapinlac HA, et al. Clinical staging of patients with early esophageal adenocarcinoma: does FDG-PET/CT have a role? J Thorac Oncol 2014; 9(8):1202–1206. doi:10.1097/JTO.0000000000000222
24. Little SG, Rice TW, Bybel B, et al. Is FDG-PET indicated for superfi cial esophageal cancer? Eur J Cardiothorac Surg 2007; 31(5):791–796. doi:10.1016/j.ejcts.2007.01.037
25. Choi J, Chung H, Lee A, Kim JL, Cho SJ, Kim SG. Role of endoscopic ultrasound in selecting superfi cial esophageal cancers for endoscopic resection. Ann Thorac Surg 2021; 111(5):1689–1695. doi:10.1016/j. athoracsur.2020.07.029
26. Espinoza-Mercado F, Imai TA, Borgella JD, et al. Does the approach matter? Comparing survival in robotic, minimally invasive, and open esophagectomies. Ann Thorac Surg 2019; 107(2):378–385. doi:10.1016/j.athoracsur.2018.08.039
27. Newton AD, Predina JD, Xia L, et al. Surgical management of earlystage esophageal adenocarcinoma based on lymph node metastasis risk. Ann Surg Oncol 2018; 25(1):318–325. doi:10.1245/s10434-017-6238-z
28. Otaki F, Ma GK, Krigel A, et al. Outcomes of patients with submucosal (T1b) esophageal adenocarcinoma: a multicenter cohort study. Gastrointest Endosc 2020; 92(1):31–39.e1. doi:10.1016/j.gie.2020.01.013
29. Yang J, Lu Z, Li L, et al. Relationship of lymphovascular invasion with lymph node metastasis and prognosis in superfi cial esophageal carcinoma: systematic review and meta-analysis. BMC Cancer 2020; 20(1):176. doi:10.1186/s12885-020-6656-3
30. Raja S, Rice TW, Goldblum JR, et al. Esophageal submucosa: the watershed for esophageal cancer. J Thorac Cardiovasc Surg 2011; 142(6):1403–1411.e1. doi:10.1016/j.jtcvs.2011.09.027
31. Seder CW, Wright CD, Chang AC, Han JM, McDonald D, Kozower BD. The Society of Thoracic Surgeons General Thoracic Surgery Database Update on Outcomes and Quality. Ann Thorac Surg 2016; 101(5):1646–1654. doi:10.1016/j.athoracsur.2016.02.099
32. Zhang YM, Boerwinkel DF, Qin X, et al. A randomized trial comparing multiband mucosectomy and cap-assisted endoscopic resection for endoscopic piecemeal resection of early squamous neoplasia of the esophagus. Endoscopy 2016; 48(4):330–338. doi:10.1055/s-0034-1393358
33. Mejia Perez LK, Yang D, Draganov PV, et al. Endoscopic submucosal dissection vs endoscopic mucosal resection for early Barrett’s neoplasia in the West: a retrospective study. Endoscopy 2021; 10.1055/ a–1541–7659. doi:10.1055/a-1541-7659
34. Peng W, Tan S, Ren Y, et al. Effi cacy and safety of endoscopic submucosal tunnel dissection for superfi cial esophageal neoplastic lesions: a systematic review and meta-analysis. J Cardiothorac Surg 2020; 15(1):33. doi:10.1186/s13019-020-1074-9
35. Mejia Perez LK, Alaber O, Jawaid S, et al. Mo1204 Endoscopic submucosal dissection vs endoscopic mucosal resection for treatment of Barrett’s related superfi cial esophageal neoplasia: retrospective multicenter study. Gastrointest Endosc 2019; 89(6):AB462–AB3.
36. Joseph A, Draganov P, Maluf-Filho F, et al. Outcomes for ESD of pathologically staged T1b esophageal cancer: a multi-center study Gastrointest Endosc 2022; S0016-5107(22)00123-7. doi:10.1016/j. gie.2022.02.018
37. Terheggen G, Horn EM, Vieth M, et al. A randomised trial of endoscopic submucosal dissection versus endoscopic mucosal resection for early Barrett’s neoplasia. Gut 2017; 66(5):783–793. doi:10.1136/gutjnl-2015-310126
38. Guo HM, Zhang XQ, Chen M, Huang SL, Zou XP. Endoscopic submucosal dissection vs endoscopic mucosal resection for superfi cial esophageal cancer. World J Gastroenterol 2014; 20(18):5540–5547. doi:10.3748/wjg.v20.i18.5540
39. Mejía-Pérez LK, Abe S, Stevens T, et al. A minimally invasive treatment for early GI cancers. Cleve Clin J Med 2017; 84(9):707–717. doi:10.3949/ccjm.84a.16063
40. Shapiro J, van Lanschot JJB, Hulshof MCCM, et al. Neoadjuvant chemoradiotherapy plus surgery versus surgery alone for oesophageal or junctional cancer (CROSS): long-term results of a randomised controlled trial. Lancet Oncol 2015; 16(9):1090–1098. doi:10.1016/S1470-2045(15)00040-6
41. Messager M, Mirabel X, Tresch E, et al. Preoperative chemoradiation with paclitaxel-carboplatin or with fl uorouracil-oxaliplatin-folinic acid (FOLFOX) for resectable esophageal and junctional cancer: the PROTECT-1402, randomized phase 2 trial. BMC Cancer 2016; 16:318. doi:10.1186/s12885-016-2335-9
42. Zhang Y, Liu L, Wang Q, et al. Endoscopic submucosal dissection with additional radiotherapy in the treatment of T1a esophageal squamous cell cancer: randomized controlled trial. Endoscopy 2020; 52(12):1066–1074. doi:10.1055/a-1198-5232
43. Pimentel-Nunes P, Dinis-Ribeiro M, Ponchon T, et al. Endoscopic submucosal dissection: European Society of Gastrointestinal Endoscopy (ESGE) guideline. Endoscopy 2015; 47(9):829–854. doi:10.1055/s-0034-1392882
44. Standards of Practice Committee, Wani S, Qumseya B, et al. Endoscopic eradication therapy for patients with Barrett’s esophagusassociated dysplasia and intramucosal cancer. Gastrointest Endosc 2018; 87(4):907–931.e9. doi:10.1016/j.gie.2017.10.011
45. Bhatt A, Kamath S, Murthy SC, Raja S. Multidisciplinary evaluation and management of early stage esophageal cancer. Surg Oncol Clin N Am 2020; 29(4):613–630. doi:10.1016/j.soc.2020.06.011